Molybdenan sodný
| Molybdenan sodný | |
|---|---|
 Vzhled | |
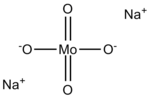 Strukturní vzorec | |
 Krystalická struktura dihydrátu | |
| Obecné | |
| Systematický název | molybdenan sodný |
| Ostatní názvy | molybdenan disodný |
| Anglický název | Sodium molybdate Disodium molybdate |
| Německý název | Natriummolybdat |
| Sumární vzorec | Na2MoO4 |
| Vzhled | bílý prášek |
| Identifikace | |
| Registrační číslo CAS | 7631-95-0 10102-40-6 (dihydrát) |
| EC-no (EINECS/ELINCS/NLP) | 231-551-7 |
| PubChem | 4384450 |
| Číslo RTECS | QA5075000 |
| Vlastnosti | |
| Molární hmotnost | 205,92 g/mol (bezvodý) 241,95 g/mol (dihydrát) |
| Teplota tání | 687 °C |
| Hustota | 3,780 g/cm3 |
| Index lomu | 1,714 |
| Rozpustnost ve vodě | 84 g/100 ml (100 °C) |
| Bezpečnost | |
 GHS07 Varování[1] | |
| NFPA 704 |  0 2 0 |
| Teplota vznícení | nehořlavý |
Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). Některá data mohou pocházet z datové položky. | |
Molybdenan sodný (Na2MoO4) je sodná sůl kyseliny molybdenové. Často se vyskytuje jako dihydrát Na2MoO4·2H2O.
Příprava
Molybdenan sodný se připravuje rozpouštěním oxidu molybdenového v roztoku hydroxidu sodného při 50–70 °C, krystalizací a filtrací,[2] bezvodá forma se připravuje zahřátím na 100 °C:
- MoO3 + 2 NaOH → Na2MoO4·2H2O
Použití
Na2MoO4 se dá použít jako zdroj molybdenu.
V zemědělství se jej spotřebuje 450 tun ročně jako umělé hnojivo, například pro pěstování brokolice nebo květáku. Potravinářský průmysl ho používá pro výrobu některých potravinových doplňků.[3]
Dále se používá v průmyslu jako inhibitor koroze.[2]
Struktura
Molybdenanový aniont má tetraedrickou strukturu, na každý aniont připadají dva kationty sodíku.[2]
Reakce
Reakcí s tetrahydridoboritanem sodným se molybden redukuje na oxid molybdeničitý:[4]
- Na2MoO4 + NaBH4 + 2 H2O → NaBO2 + MoO2 + 2 NaOH + 3 H2
Molybdenan sodný také reaguje s dithiofosforečnanovými kyselinami[2]:
- Na2MoO4 + (RO)2PS2H → [MoO2(S2P(OR)2)2] (R = Me, Et)
které dále reagují za vzniku [MoO3(S2P(OR)2)4].
Bezpečnost
Molybdenan sodný nesmí přijít do styku s alkalickými kovy, většinou běžných kovů a oxidačními činidly. Při dotyku s roztaveným hořčíkem exploduje, nebezpečně reaguje s interhalogeny (fluorid jodistý, fluorid bromičný atd.).[5]
Reference
V tomto článku byl použit překlad textu z článku Sodium molybdate na anglické Wikipedii.
- ↑ a b Sodium molybdate. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ a b c d Braithwaite, E.R.; Haber, J. Molybdenum: An outline of its Chemistry and Uses. 1994. Elsevier Science B.V. Amsterdam, The Netherlands.
- ↑ Molybden z potravin tělu stačí. Nejsme v Íránu
- ↑ Chi Fo Tsang and Arumugam Manthiram. Journal of Materials Chemistry 1997. 7(6). 1003–1006.
- ↑ http://www.mallbaker.com/americas/msds/english/s4394_msds_us_default.pdf[nedostupný zdroj]
Externí odkazy
 Obrázky, zvuky či videa k tématu Molybdenan sodný na Wikimedia Commons
Obrázky, zvuky či videa k tématu Molybdenan sodný na Wikimedia Commons - http://lpi.oregonstate.edu/infocenter/minerals/molybdenum/
| Anorganické soli sodné | |
|---|---|
| Halogenidy a pseudohalogenidy | Fluorid sodný (NaF) • Hydrogendifluorid sodný (NaHF2) • Bromid sodný (NaBr) • Chlorid sodný (NaCl) • Jodid sodný (NaI) • Kyanid sodný (NaCN) • Kyanatan sodný (NaOCN) • Isokyanát sodný (NaNCO) • Thiokyanatan sodný (NaSCN) |
| Soli kyslíkatých kyselin (neuvedeny soli | Chlornan sodný (NaOCl) • Chloritan sodný (NaClO2) • Chlorečnan sodný (NaClO3) • Chloristan sodný (NaClO4) • Bromnan sodný (NaOBr) • Bromitan sodný (NaBrO2) • Bromičnan sodný (NaBrO3) • Jodičnan sodný (NaIO3) Jodistan sodný (NaIO4) • Siřičitan sodný (Na2SO3) • Hydrogensiřičitan sodný (NaHSO3) • Disiřičitan sodný (Na2S2O5) • Dithioničitan sodný (Na2S2O4) • Dithionan sodný (Na2S2O6) • Síran sodný (Na2SO4) • Hydrogensíran sodný (NaHSO4) • Disíran sodný (Na2S2O7) • Peroxosíran sodný (Na2SO5) • Peroxodisíran sodný (Na2S2O8) • Seleničitan sodný (Na2SeO3) • Selenan sodný (Na2SeO4) • Telluričitan sodný (Na2TeO3) • Metatelluran sodný (Na2TeO4) • Pentahydrogenorthotelluran sodný (NaH5TeO6) • Cis-dusnan sodný (Na2N2O2) • Trans-dusnan sodný (Na2N2O2) • Peroxodusnan sodný (NaONNOONa; Na2N2O3) • Dusitan sodný (NaNO2) • Dusičnan sodný (NaNO3) • Orthodusičnan sodný (Na3NO4) • Peroxodusitan sodný (NaOONO) • Fosfornan sodný (NaPO2H2) • Dihydrogenfosforitan sodný (NaH2PO3) • Hydrogenfosforitan sodný (Na2HPO3) • Dihydrogenfosforečnan sodný (NaH2PO4) • Hydrogenfosforečnan sodný (Na2HPO4) • Fosforečnan sodný (Na3PO4) • Dihydrogendifosforečnan disodný (Na2H2P2O7) • Hydrogendifosforečnan trisodný (Na3HP2O7) • Difosforečnan sodný (Na4P2O7) • Trifosforečnan sodný (Na5P3O10) • Metafosforečnan sodný (NaPO3) • Cyklotrifosforečnan sodný (Na3P3O9) • Cyklohexafosforečnan sodný (Na6P6O18) • Arsenitan sodný (NaAsO2) • Hydrogenarseničnan sodný (Na2HAsO4) • Arseničnan sodný (Na3AsO4) • Tetrahydrogenantimonitan sodný (NaSb (OH)4) • Antimonitan sodný (NaSbO2) • Bismutičnan sodný (NaBiO3) • Uhličitan sodný (Na2CO3) • Hydrogenuhličitan sodný (NaHCO3) • Šťavelan sodný (Na2(CO2)2) • Hydrogenšťavelan sodný (NaH(CO2)2) • Orthokřemičitan sodný (Na4SiO4) • Metakřemičitan sodný (~Na2SiO3~) • Dikřemičitan sodný (Na2Si2O5) • Trikřemičitan sodný (Na2Si3O7) • Cínatan sodný (Na2SnO2) • Cíničitan sodný (Na2SnO3) • Metaboritan sodný (NaBO2) • Tetraboritan sodný (Na2[B4O5(OH)4]•8H2O) • Oktaboritan sodný (Na2B8O13•4H2O) • Perboritan sodný (Na2H4B2O8) • Hlinitan sodný (Na3AlO3) • Tetrahydroxidozinečnatan sodný (Na2Zn(OH)4) • Zinečnatan sodný (Na2ZnO2) • Rtuťnatan sodný (Na2HgO2) • Železičitan sodný (Na2FeO3) • Železan sodný (Na2FeO4) • Manganitan sodný (~NaMnO2~) • Manganečnan sodný (Na3MnO4) • Manganan sodný (Na2MnO4) • Manganistan sodný (NaMnO4) • Technecistan sodný (NaTcO4) • Rhenistan sodný (NaReO4) • Chromitan sodný (Na3[Cr(OH)6]) • Chroman sodný (Na2CrO4) • Dichroman sodný (Na2Cr2O7) • Molybdenan sodný (Na2MoO4) • Wolframan sodný (Na2WO4) • Metavanadičnan sodný (NaVO3) • Orthovanadičnan sodný (Na3VO4) • Trititaničitan sodný (Na2Ti3O7) • Zirkoničitan sodný (Na2ZrO3) • Diuranan sodný (Na2U2O7) |
| Soli tvořené záměnou vodíku ze sloučenin typu prvekx – vodíky | Hydrid sodný (NaH) • Hydroxid sodný (NaOH) • Oxid sodný (Na2O) • Peroxid sodný (Na2O2) • Superoxid sodný (NaO2) • Hydrogensulfid sodný (NaSH) • Sulfid sodný (Na2S) • Polysulfid sodný (Na2Sn) • Selenid sodný (Na2Se) • Tellurid sodný (Na2Te) • Polonid sodný (Na2Po) • Amid sodný (NaNH2) • Imid sodný (Na2NH) • Nitrid sodný (Na3N) • Azid sodný (NaN3) • Fosfid sodný (Na3P) • Dihydrogenarsenid sodný (NaAsH2) • Tetrahydridoboritan sodný (NaBH4) • Tetrahydridohlinitan sodný (NaAlH4) |
| Jiné | |











