Кофермент A
| Кофермент A | |
|---|---|
  | |
| Общие | |
| Систематическое наименование | '"`UNIQ--nowiki-00000000-QINU`"' |
| Традиционные названия | кофермент A |
| Хим. формула | C21H36N7O16P3S |
| Физические свойства | |
| Молярная масса | 767,534 ± 0,031 г/моль |
| Классификация | |
| Рег. номер CAS | 85-61-0 |
| PubChem | 68163312 |
| Рег. номер EINECS | 201-619-0 |
| SMILES | O=C(NCCS)CCNC(=O)C(O)C(C)(C)COP(=O)(O)OP(=O)(O)OC[C@H]3O[C@@H](n2cnc1c(ncnc12)N)[C@H](O)[C@@H]3OP(=O)(O)O |
| InChI | InChI=1S/C21H36N7O16P3S/c1-21(2,16(31)19(32)24-4-3-12(29)23-5-6-48)8-41-47(38,39)44-46(36,37)40-7-11-15(43-45(33,34)35)14(30)20(42-11)28-10-27-13-17(22)25-9-26-18(13)28/h9-11,14-16,20,30-31,48H,3-8H2,1-2H3,(H,23,29)(H,24,32)(H,36,37)(H,38,39)(H2,22,25,26)(H2,33,34,35)/t11-,14-,15-,16+,20-/m1/s1 RGJOEKWQDUBAIZ-IBOSZNHHSA-N |
| ChEBI | 15346 |
| ChemSpider | 79067 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
 Медиафайлы на Викискладе Медиафайлы на Викискладе | |
Кофермент A (коэнзим A, КоA, СоА, HSKoA) — кофермент ацетилирования; один из важнейших коферментов, принимающий участие в реакциях переноса ацильных групп при синтезе и окислении жирных кислот и окислении пирувата в цикле лимонной кислоты.[1]
Строение
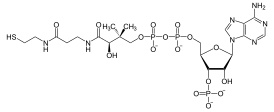
Молекула кофермента A состоит из остатка адениловой кислоты (1), связанной пирофосфатной группой (2) с остатком пантоевой кислоты (3), которая в свою очередь связана амидной связью с аминокислотой β-аланином (4) (эти две группы представляют собой остаток пантотеновой кислоты), соединённой амидной связью с остатком β-меркаптоэтаноламина (5).
Биосинтез
Кофермент A синтезируется в пять этапов из пантотеновой кислоты (витамина B5) и цистеина:
- Пантотеновая кислота фосфорилируется в 4'-фосфопантотенат с помощью фермента пантотенаткиназы
- Цистеин присоединяется к 4'-фосфопантотенату с помощью фермента фосфопантотеноилцистеинсинтетазы с образованием 4'-фосфо-N-пантотеноилцистеина
- 4'-фосфо-N-пантотеноилцистеин декарбоксилируется с образованием 4'-фосфопантотеина с помощью фермента фосфопантотеноилцистеиндекарбоксилазы
- 4'-фосфопантотеин с адениловой кислотой формирует дефосфо-КоA под действием фермента фосфопантотеинаденилтрансферазы
- Наконец, дефосфо-КоA фосфорилируется АТФ в кофермент A с помощью фермента дефосфокоэнзимкиназы.
Биохимическая роль
С КоА связан ряд биохимических реакций, лежащих в основе окисления и синтеза жирных кислот, биосинтеза жиров, окислительных превращений продуктов распада углеводов. Во всех случаях КоA действует в качестве промежуточного звена, связывающего и переносящего кислотные остатки на другие вещества. При этом кислотные остатки в составе соединения с КоA подвергаются тем или иным превращениям, либо передаются без изменений на определённые метаболиты.
История открытия
Впервые кофермент был выделен из печени голубя в 1947 году Ф. Липманом[2]. Структура кофермента A была определена в начале 1950-х годов Ф. Линеном в Институте Листера в Лондоне. Полный синтез КоA осуществил в 1961 году X. Корана.
Список ацил-КоA
Из природных соединений выделены и идентифицированы различные ацильные производные кофермента A:
Ацил-КоA из карбоновых кислот:
- Ацетил-КоА
- Пропионил-КоА
- Ацетоацетил-КоА
- Кумарол-КоА
- Бутирил-КоА
Ацил-КоА из дикарбоновых кислот:
- Малонил-КоА
- Сукцинил-КоА
- Гидроксиметилглютарил-КоА
- Пименил-КоА
Ацил-КоА из карбоциклических кислот:
- Бензоил-КоА
- Фенилацетил-КоА
Существуют также разнообразные ацил-КоА жирных кислот, которые играют большую роль в качестве субстратов для реакций синтеза липидов.
См. также
- Витамин B5
Примечания
Литература
- Филиппович, Ю. Б. Основы биохимии: Учеб. для хим. и биол. спец. пед. ун-тов и ин-тов / Ю. Б. Филиппович. — 4-е изд., перераб. и доп. — М.: «Агар», 1999. — 512 с., ил.
- Березов, Т. Т. Биологическая химия: Учебник / Т. Т. Березов, Б. Ф. Коровкин. — 3-е изд., перераб. и доп. — М.: Медицина, 1998. — 704 с., ил.
- Овчинников, Ю. А. Биоорганическая химия / Ю. А. Овчинников. — М.: Просвещение, 1987. — 815 с., ил.
- Племенков, В. В. Введение в химию природных соединений / В. В. Племенков. — Казань: КГУ, 2001. — 376 с.










