Karbonilna grupa

U organskoj hemiji, karbonilna grupa je familija funkcionalnih grupa koje se sastoje od ugljenikovog atoma dvostruko-vezanog za kiseonikov atom: C=O.[1]
Termin karbonil se takođe može odnositi na ugljen-monoksid kao ligand u neorganskim ili organometalnim kompleksima (metalni karbonil, npr. nikl-tetrakarbonil).
Karbonilna jedinjenja
Karbonilna grupa karakteriše sledeće tipove jedinjenja:
| Jedinjenje | Aldehid | Keton | Karboksilna kiselina | Estar | Amid | Enon | Acil halid | Acil anhidrid |
| Struktura | 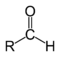 |  |  |  |  |  |  |  |
| Generalna formula | RCHO | RCOR' | RCOOH | RCOOR' | RCONR'R'' | RC(O)C(R')CR''R''' | RCOX | (RCO)2O |
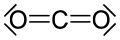
Drugi organski karbonili su ureja i karbamati, derivati acil hlorida: hloroformati i fosgen, karbonatni estri, tioestri, laktoni, laktami, hidroksamati, i izocijanati. Primeri neorganskih karbonilnih jedinjenja su ugljen-dioksid i karbonil-sulfid.
Specijalna grupa karbonilnih jedinjenja su 1,3-dikarbonil jedinjenja koja imaju kisele protone na centralnoj metilenskoj jedinici. Primeri su Meldrumska kiselina, dietil malonat i acetilaceton.
Reaktivnost

Kiseonik je elektronegativniji od ugljenika, tako da odvlači elektronsku gustinu sa ugljenika čime povećava polarnost veze. Karbonilni ugljenik postaje elektrofilan, i stoga lakše reaguje sa nukleofilima. Isto tako, elektronegativni kiseonik može da reaguje sa elektrofilima; na primer sa protonom iz kiselog rastvora ili drugim Luisovim kiselinama.
Alfa vodonici karbonilnog jedinjenja su znatno kiseliji (~103 puta kiseliji) nego u vodonici tipične C-H veze. Na primer, pKa vrednosti acetaldehida i acetona su 16.7 i 19, respektivno.[2] Karbonil je u tautomernoj rezonanci sa enolom. Deprotonacija enola jakom bazom proizvodi enolat, koji je snažan nukleofil i može da alkiluje elektrofile kao što su drugi karbonili.
Reference
Literatura
Dodatna literatura
- L.G. Wade, Jr (2002). Organic Chemistry (5th изд.). Prentice Hall. ISBN 978-0-13-033832-7.
- The Frostburg State University Chemistry Department. Organic Chemistry Help (2000).
- Advanced Chemistry Development, Inc. IUPAC Nomenclature of Organic Chemistry (1997).
- William Reusch. tara VirtualText of Organic Chemistry (2004).
- Purdue Chemistry Department [1] (retrieved Sep 2006). Includes water solubility data.
- William Reusch. (2004) Aldehydes and Ketones Архивирано на сајту Wayback Machine (30. април 2010), Приступљено 23. 5. 2005.
- ILPI. (2005) The MSDS Hyperglossary- Anhydride.
- п
- р
- у
Alkohol · Aldehid · Alkan · Alken · Alkin · Amid · Amidin · Amin · Azo jedinjenje · Derivat benzena · Karboksil · Cijanat · Disulfid · Estar · Etar · Haloalkan · Hidrazon · Imid · Imin · Izocijanid · Izocijanat · Izonitril · Izotiocijanat · Karbamat · Keton · Organofosfor · Oksim · Nitril · Nitro · Nitrozo · Peroksid · Fosfonit · Fosfonat · Derivat piridina · Sulfon · Sulfonska kiselina · Sulfoksid · Tiocijanat · Tioestar · Tioetar · Tiol









